Indikasyon (aprobahan nga paggamit): Sa 2019, giaprobahan kini sa FDA alang sa pagtambal sa naangkon, generalized hypoactive sexual desire disorder (HSDD) sa mga babaye nga premenopausal kung ang kondisyon maoy hinungdan sa grabeng kagul-anan ug dili tungod sa ubang medikal/psychiatric nga kondisyon o epekto sa droga.
Mekanismo sa Aksyon
Ang PT-141 usa ka melanocortin receptor agonist (panguna nga MC4 receptor) nga nag-modulate sa sekswal nga tinguha pinaagi sa mga agianan sa sentral nga sistema sa nerbiyos.
Dili sama sa PDE5 inhibitors (pananglitan, sildenafil), nga nag-una nga makaapekto sa mga ugat sa dugo, ang PT-141 nagtrabaho sa sentro aron makaapekto sa sekswal nga kadasig ug pagpukaw.
Pharmacology & Dosing
Pagdumala: Subcutaneous injection, kung gikinahanglan (on-demand).
Giaprobahan nga dosis: 1.75 mg sc
Pharmacokinetics:
Tmax ≈ ~60 ka minuto
t½ ≈ 2–3 ka oras
Ang mga epekto mahimong molungtad sa daghang oras, sa pipila ka mga taho hangtod sa ~16 ka oras.
Pagkaepektibo sa Klinikal (Mga Pagsulay sa Yugto III - PAG-RECONNECT, 24 ka semana, RCTs)
Panguna nga mga endpoint:
Female Sexual Function Index–Desire domain (FSFI-D)
Babaye nga Sekswal nga Distress Scale (FSDS-DAO)
Pangunang mga resulta (gipundok nga mga pagtuon 301 + 302):
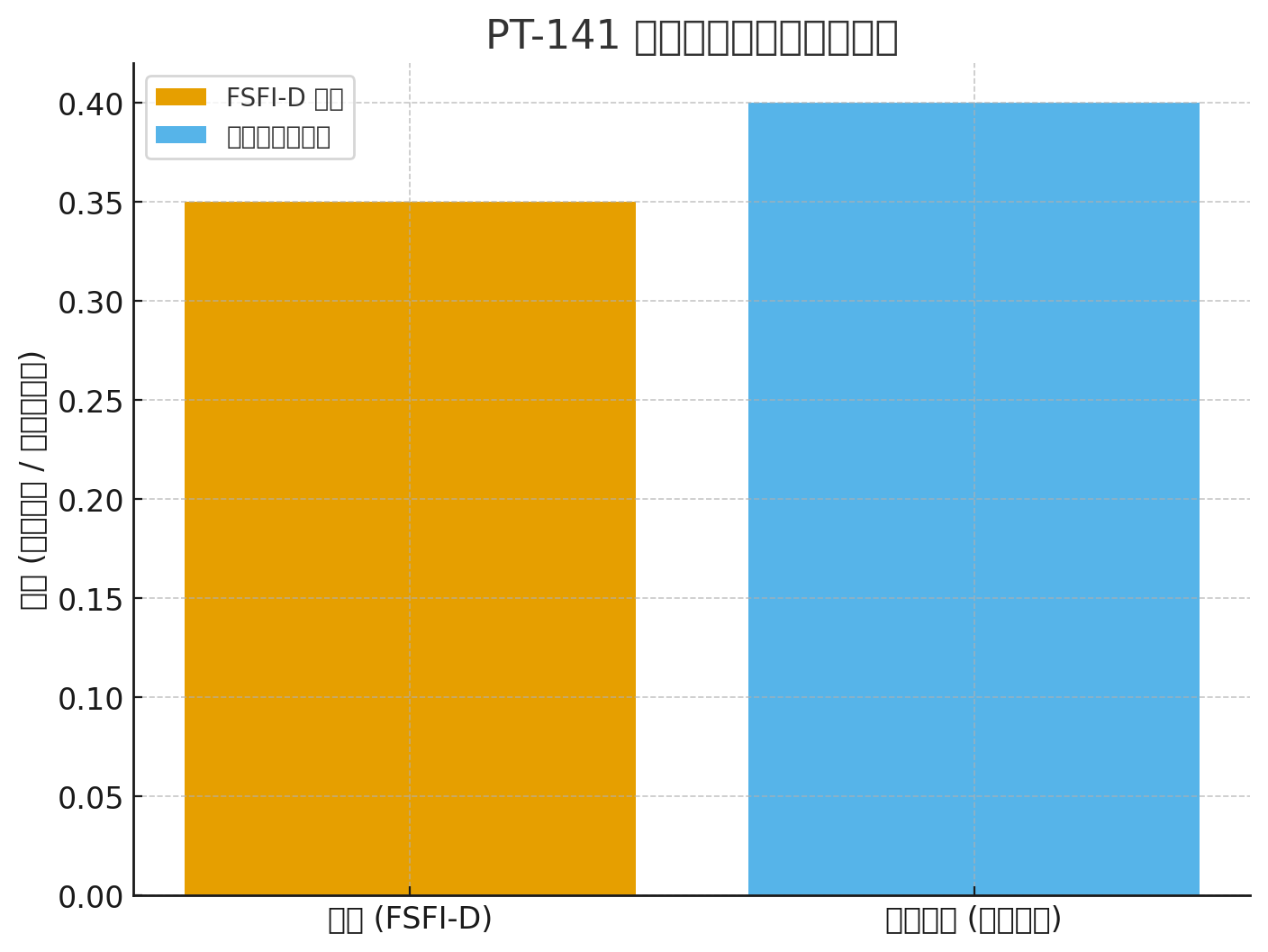
Pag-uswag sa FSFI-D: +0.35 vs placebo (P<0.001)
Pagkunhod sa marka sa FSDS-DAO: −0.33 vs placebo (P<0.001)
Ubang mga endpoint: Ang mga resulta sa pagsuporta (mga marka sa sekswal nga function, katagbawan nga gitaho sa pasyente) nag-uswag nga positibo, apan ang makatagbaw nga mga panghitabo sa sekso (SSEs) dili kanunay nagpakita sa makanunayon nga mahinungdanong mga kalainan.
Dili maayo nga mga Panghitabo (labing kanunay nga gitaho sa mga pagsulay)
Kasagaran (≥10%):
Kasukaon (~ 30–40%; hangtod sa ~40% nga gitaho sa mga pagsulay)
Pag-flush (≥10%)
Sakit sa ulo (≥10%)
Mga epekto sa cardiovascular:
Ang lumalabay nga pagtaas sa presyon sa dugo ug mga kausaban sa pitik sa kasingkasing naobserbahan, kasagarang masulbad sulod sa pipila ka oras.
Contraindicated o gigamit uban ang pag-amping sa mga pasyente nga adunay dili makontrol nga hypertension o sakit sa cardiovascular.
Atay: Talagsa nga mga taho sa lumalabay nga pagtaas sa enzyme sa atay; talagsa ra nga mga taho sa kaso nagsugyot nga posible nga mahait nga kadaot sa atay, apan dili kasagaran.
Dugay nga Kaluwasan (Extension nga Pagtuon)
Ang usa ka 52-semana nga open-label extension nga pagtuon nakit-an nga nagpadayon nga mga pag-uswag sa tinguha nga wala’y bag-ong dagkong mga signal sa kaluwasan.
Ang long-term nga profile sa kaluwasan nga gikonsiderar sa kasagaran maayo nga pagtugot, nga ang mga nag-unang mga isyu sa pagkamatugtanon mao gihapon ang dili maayo nga mga epekto sama sa kasukaon.
Panguna nga mga Nota sa Paggamit
Limitado ang giaprobahan nga populasyon: Para lamang sa mga babaye nga premenopausal nga adunay nakuha, generalized nga HSDD.
Dili kaylap nga giaprobahan alang sa mga lalaki (ED o ubos nga tinguha sa mga lalaki nagpabilin nga imbestigasyon).
Ang pag-screen sa kaluwasan hinungdanon: Ang hypertension, sakit sa cardiovascular, ug kasaysayan sa atay kinahanglan nga susihon sa wala pa magreseta.
Dali nga Summary sa Data
Pag-apruba sa FDA: 2019 (Vyleesi).
Dosis: 1.75 mg subcutaneous indeyksiyon, sa panginahanglan.
PK: Tmax ~60 min; t½ 2–3 ka oras; epekto hangtod sa ~16 h.
Kaepektibo (Phase III, gipundok):
FSFI-D: +0.35 (P<.001)
FSDS-DAO: −0.33 (P<.001)
Dili maayo nga mga panghitabo:
Kasukaon: hangtod sa ~40%
Pag-flush: ≥10%
Sakit sa ulo: ≥10%
Ang lumalabay nga pagtaas sa BP namatikdan.
Comparative Table ug Graph (Sumaryo)
| Pagtuon / Type sa Data | Katapusan nga Punto / Sukdanan | Bili / Deskripsyon |
|---|---|---|
| Yugto III (301+302 gipundok) | FSFI-D (desire domain) | +0.35 batok sa placebo (P<0.001); FSDS-DAO −0.33 |
| Dili Maayo nga mga Hitabo | Kasukaon, labad, labad sa ulo | Kasukaon ~30–40% (max ~40%); paghugas ≥10%; labad sa ulo ≥10% |
Oras sa pag-post: Sep-30-2025